Гены фолатного цикла и бесплодие
27 декабря 2017 г.
Как только у женщины появляются мысли стать мамой, то она обращается в женскую консультацию для полного обследования. И в первую очередь врач назначает фолиевую кислоту. Насколько важна роль этого витамина для организма, что такое фолатный цикл и в чем заключается опасность при полиморфизме генов?
Полиморфизмы генов фолатного цикла: что это такое?
Для начала разберемся, что такое полиморфизм генов. Гены у разных людей похожи, но имеют небольшие нюансы, которые и отличают нас друг от друга. Эти нюансы, различия и называются полиморфизмами.
Причиной полиморфизма генов являются изменения отдельных участков в молекуле ДНК, что приводит к изменению свойств гена (иногда в лучшую, а иногда – в худшую сторону). Некоторые изменения ведут к генетическим заболеваниям, другие не влекут за собой болезни, но являются фактором предрасположенности к ряду патологий.
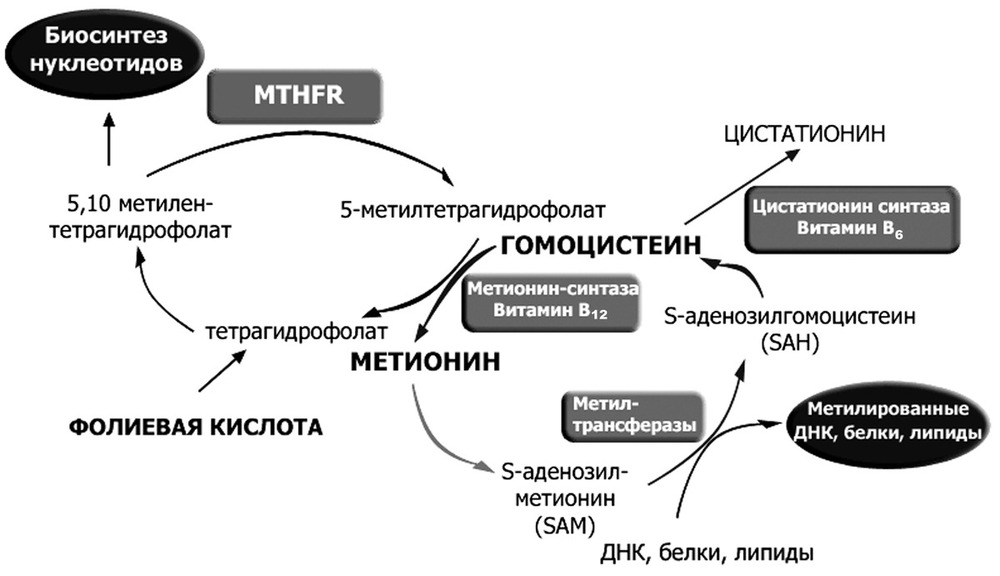
А что же такое фолатный цикл? Фолатный цикл – это совокупность процессов, в результате которых при помощи ферментов и коферментов из гомоцистеина появляется незаменимая аминокислота метионин.
Ферменты – это вещества, ускоряющие биохимические процессы в организме. В фолатном цикле принимают участие 3 фермента:
- метилентетрагидрофолатредуктаза MTHFR (для перевода фолиевой кислоты в активную форму);
- метионин-синтаза-редуктаза MTRR (влияет на активность метионин-синтазы);
- метионин-синтаза MTR (осуществляет превращение гомоцистеина);
Коферменты – это производные витаминов, необходимые для функционирования ферментов.
Коферментами являются фолаты, а для обмена фолатов необходимы витамины:
- В9 (фолиевая кислота);
- В6 (пиридоксин);
- В12 (цианокобаламин).
Фолатный цикл обеспечивает нормальное функционирование органов и систем. При мутации в генах происходит замена одного нуклеотида на другой, изменения числа повторяющихся фрагментов ДНК. Это все ведет к изменению биохимических свойств фермента и его функции, в результате чего нарушается превращение гомоцистеина в метионин.
Сбой в фолатном цикле влечет за собой увеличение концентрации в крови гомоцистеина, оказывающего на организм токсическое, атерогенное и тромбофиличское действие. Иными словами, возрастает риск некоторых осложнений беременности (например, гестоза или отслоения плаценты) и возникновения дефектов у плода.

Из-за чего может нарушиться метаболизм гомоцистеина и произойти сбой в фолатном цикле?
- генетические дефекты ферментов;
- дефицит витаминов вследствие недостаточного поступления с пищей или на фоне приема лекарственных средств (эстрогенсодержащих оральных контрацептивов, цитостатиков, противоэпилептических средств).
Кроме того, повышенный уровень гомоцистеина может быть при хронических заболеваниях: почечной недостаточности, анемии, псориазе, гипотиреозе; злокачественных опухолях яичников, молочной и поджелудочной желез.
Информация о ферментах фолатного цикла (MTHFR, MTRR, MTR) содержится в генах, которые именуются генами фолатного цикла. Эти гены могут иметь свои особенности у каждого человека – полиморфизмы. Исследование полиморфизмов в таких генах способно выявить, есть ли в конкретном случае риск нарушения фолатного цикла.
Важно! Не все полиморфизмы в генах фолатного цикла могут приводить к повышению гомоцистеина.
Диагностика полиморфизмов генов фолатного цикла
Исследование на полиморфизм генов фолатного цикла проводят методом полимеразной цепной реакции. Кровь для анализа лучше сдавать утром натощак, последний прием пищи должен быть накануне вечером.
Расшифровку данных полиморфизма генов фолатного цикла (MTR, MTRR, MTHFR) проводит только врач. Даже при выявленном полиморфизме не надо отчаиваться – это говорит только о предрасположенности к заболеванию и не означает, что в течение беременности обязательно будут осложнения.
Полиморфизмы генов фолатного цикла: в чем риск для матери и плода?
Уровень гомоцистеина при нормально протекающей беременности чуть понижается, составляя 4,6-12,4 мкмоль/л, и восстанавливается только после родов. Но при нарушениях в фолатном цикле он повышается и может оказывать токсическое, тромбофилическое и атерогенное действие.
Все это приводит к развитию различных патологических процессов со стороны матери и плода:
- угроза прерывания беременности;
- неудачное ЭКО;
- неразвивающаяся беременность;
- фетоплацентарная недостаточность;
- хроническая внутриутробная гипоксия плода;
- поздний гестоз;
- внутриутробная задержка роста и развития плода;
- пороки развития плода (дефекты нервной трубки, деформация лицевого скелета с незаращением неба и верхней губы, анэнцефалия);
- повышается риск развития синдрома Дауна.
Планирование беременности при полиморфизмах генов фолатного цикла
При планировании беременности важно выявить возможные хромосомные аномалии, в том числе носительство полиморфизма генов гемостаза и фолатного цикла.
Чтобы исключить наличие какой-либо патологии, обязательно надо посетить акушера-гинеколога. При опросе врач досконально соберет анамнез и при необходимости назначит дополнительное обследование, консультацию генетика.
Уровень гомоцистеина проверяют, если:
- предыдущие беременности завершились неблагоприятным исходом;
- у женщины повышенная свертываемость крови;
- у родственников будущей мамы были тромбозы, инфаркты или инсульты до 50 лет.
Важно! В течение 2-3 месяцев до зачатия всем женщинам совместно с партнером рекомендуют пропить фолиевую кислоту в профилактической дозе 0,4 мг/сутки.
Ведение беременности при полиморфизмах генов фолатного цикла
При наступлении беременности фолиевую кислоту продолжают пить до 12 недель включительно, что обеспечивает снижение риска нарушений со стороны нервной системы плода. Витамин выпускается в таблетках по 1 мг, назначают по 1 таб/сутки.
При полиморфизме дозировка может увеличиваться до 5 мг/сутки, а прием продолжают в течение всей беременности совместно с витаминами группы В. В критические сроки проводят дополнительную терапию.
Врач-генетик может порекомендовать принимать не обычный В9, а фолиевую кислоту в активной форме. В чем разница? Дело в том, что в чистом виде фолиевая кислота организмом не усваивается – для этого она должна преобразоваться в определенную форму – метилфолат. При мутации некоторых генов процесс превращения В9 в усвояемую форму нарушен, поэтому обычная фолиевая кислота усваивается плохо. В этом случае препаратом выбора становится ее активная форма – L-метилфолат, который легко всасывается в кровь без каких-либо преобразований.
Рекомендуют употреблять больше пищи с витамином В9 – шпинат, брокколи, горошек, авокадо, банан, арахис, бобовые, белый рис, хлеб из муки грубого помола, печень, мёд, томатный и апельсиновый соки.
В обязательном порядке контролируют уровень гомоцистеина в динамике, коагулограмму.
Врач-гинеколог о гомоцистеине при планировании беременности.
Роды при полиморфизмах генов фолатного цикла
В большинстве случаев на фоне профилактических мероприятий и проводимой терапии роды проходят хорошо.
Но могут быть следующие осложнения:
- преждевременные роды;
- преэклампсия, когда показано оперативное вмешательство в экстренном порядке;
- преждевременная отслойка нормально расположенной плаценты;
- кровотечение.
Главное, не переживайте и соблюдайте все рекомендации.
В послеродовом периоде до окончания кормления грудью продолжайте прием фолиевой кислоты по 0,4-1 мг/сутки.
Владлена Размерица, акушер-гинеколог, специально для Mirmam.pro

Фолиевая кислота в продуктах
Фолацин и фолиевая кислота: делаем правильный выбор

Путешествия во время беременности: польза или вред?

Как похудеть во время беременности, не навредив ребенку?
Источник
Поскольку метаболизм фолатов является важным звеном базовых биологических процессов, то его нарушения, в том числе генетически обусловленные, рассматриваются как фактор высокого риска развития патологических состояний: сердечно-сосудистых заболеваний (ССЗ), онкологических заболеваний, нарушений репродуктивных функций и патологий развития плода. Своевременное выявление генетической мутации, нарушающей выработку ферментов фолатного цикла, дает возможность эффективно контролировать и корректировать уровень фолиевой кислоты у пациентов, что благотворно сказывается на их здоровье.
Группа соединений фолатов играет ведущую роль в широком спектре жизненно важных процесов:
- Стимулирует эритропоэз
- Участвует в синтезе аминокислот, нуклеиновых кислот, пуринов, пиримидинов, витаминов
- Участвует в обмене холина, гистидина
- Является важным сопутствующим фактором в метилировании ДНК и РНК
- Способствует регенерации мышечной ткани
- Влияет на развитие быстрорастущих тканей (кожа, оболочки ЖКТ, костный мозг)
- Способствует нормальному созреванию и функционированию плаценты
- Оказывает эстрогеноподобное действие
- Выполняет защитную функцию при беременности по отношению к действию на плод тератогенных и повреждающих факторов
Фолатный цикл – каскадный процесс превращения фолиевой кислоты в доступное для усваивания организмом производное – 5-метилтетрагидрофолат. Процесс контролируется ферментом метилентетрагидрофолатредуктазой (MTHFR). Обмен фолатов является источником одноуглеродных фрагментов (метильной группы –СН3) для жизненно важных клеточных процессов: биосинтеза пуриновых нуклеотидов и превращения уридинионофосфата в тимидилат; митилирования ДНК и РНК.
С фолатным циклом сопряжён цикл образования метионина из гомоцистеина, который проходит при участии витамина В12 и двух ферментов: метионин-синтазы (MTR) и метионин-синтаза-редуктазы (MTRR).
Нарушения метаболизма фолатов влияют на стабильность ДНК двумя основными способами:
- Подавление синтеза тимидилата, в результате чего формируется несбалансированный нуклеотидный пул
- Низкий уровень S-аденозилметионина, что приводит к недостаточному метилированию ДНК и вызывает нарушение регуляции генной экспрессии
Поскольку метаболизм фолатов является важным звеном базовых биологических процессов, то его нарушения, в том числе генетически обусловленные, рассматриваются как фактор высокого риска развития патологических состояний: сердечно-сосудистых заболеваний (ССЗ), онкологических заболеваний, нарушений репродуктивных функций и патологий развития плода.
С точки зрения вклада в развитие ССЗ рассматриваются два процесса, связанные с фолатным циклом: накопление гомоцистеина и нарушение процессов метилирования ДНК.
Основным повреждающим эффектом повышения уровня гомоцистеина является активация атеротромбоза за счёт многочисленных механизмов. Установлено, что у больных с повышенным уровнем гомоцистеина риск смерти от всех сердечно-сосудистых причин был выше в 1,7 раза, от инфаркта миокарда – в 3,4 раза, от инсульта – в 4,3 раза, чем у больных с нормальным уровнем гомоцистеина. Кроме того, гомоцистеин является частичным агонистом рецепторов глицина. При таких состояниях, как инфаркт и травма мозга, когда концентрация глицина возрастает, даже незначительные концентрации гомоцистеина начинают оказывать выраженное нейротоксическое воздействие. Эффективность метаболизма гомоцистеина напрямую зависит от достаточности фолатов в организме и полноценного функционирования фермента MTHFR.
Роль генетически обусловленных нарушений метаболизма фолатов была доказана для пациентов с инфарктом миокарда и ишемическим инсультом: наличие полиморфизма MTHFR C667T было ассоциировано с тромботическими событиями. Тем не менее следует отметить, что само по себе носительство условно «неблагоприятных» аллельных вариантов генов ферментов фолатного цикла повышает риск ССЗ в случае отсутствия коррекции уровня фолатов в организме. Исследования показали, что носительство полиморфных аллелей MTHFR C667T не влияло на прогноз больных с нормальным уровнем фолиевой кислоты, в то время как при низком фолатном статусе риск основных коронарных событий был повышен на 32% у гетерозиготных носителей и на 44% у гомозиготных носителей аллели 667TT, а также была отмечена тенденция к повышению сердечно-сосудистых осложнений у носителей потенциально благоприятного «дикого» генотипа, имевших сопутствующий дефицит фолиевой кислоты.
Регулярный приём фолиевой кислоты (под контролем врача) значительно снижает содержание в крови гомоцистеина и сокращает ежегодную смертность от ССЗ.
Особую актуальность генетические дефекты фолатного цикла имеют с точки зрения развития репродуктивных проблем и пороков развития плода. Ассоциация генетических полиморфизмов ферментов фолатного цикла доказана при осложнениях беременности: фетоплацентарной недостаточности, преэклампсии, преждевременной отслойке нормально расположенной плаценты, замершей беременности, внутриутробной гибели плода, развитии гестоза. Была установлена связь с высокой частотой аномальных гинекологических и акушерских кровотечений. Примечательно, что дефекты генов ферментов фолатного цикла ассоциированы и с бесплодием у мужчин, необструктивной азооспермией и олигозооспермией.
Важно знать, что при наследственных дефектах генов ферментов фолатного цикла избыток синтетической фолиевой кислоты может ещё больше нарушить равновесие и привести к таким же последствиям для плода, как и дефицит этого витамина.
Показания к генетическому анализу:
- Повышенный уровень гомоцистеина в крови
- Невынашивание беременности, гибель плода
- Плановая подготовка к беременности
- Семейная предрасположенность к онкологическим заболеваниям
- Назначение химиотерапии
- Назначение оральных контрацептивов и гормональной заместительной терапии
- Наличие ИБС, артериальной гипертонии, атеросклероза или атеротромбоза
- Антифосфолипидный синдром, тромбоэмболия
- Рождение ребёнка с изолированными пороками нервной трубки, сердца или урогенитального тракта
При проведении генетического исследования метаболизма фолатов определяют следующие полиморфизмы:
- MTHFR: 677 С>T (Ala222Val)
- MTHFR: 1298 А>C (Glu429Ala)
- MTR: 2756 A>G (Asp919Gly)
- MTRR: 66 A>G (lle22Met)
Статья добавлена 20 ноября 2019 г.
Источник
Девочки, кто не может долго забеременеть: бхб, зб, выкидыши. Сдавайте генетические мутации, особенно фолатного цикла. Весь АФС и аутоиммуннку
Что я нашла у себя?
Реально жалею что не сдала раньше и не узнала об этом. Думала, если у меня есть ребенок, у меня нет проблем с генами. На самом деле вы не знаете, когда какой ген активируется. Они могут спать годами, мои например мутации тромбозов до сих пор спят. А вот мутации по кровотечениям периодически дает о себе знать.
1. На первом месте вылезла мутация фолатного цикла MTRR в самой ужасной гомозиготной форме.
А вообще нашли у меня 4 мутации: MTRR (66 A>G) g/g (гомозиготная) – фолатный цикл, FGB (-455 G>A) g/a (гетерозиготная) – тромбозы, F13A1 (103 G>T) g/t (гетерозиготная) – кровотечения, ITGA2 (807 C>T) c/t (гетерозиготная) – тромбозы.
Одна из мутаций не спит всю жизнь – это MTRR.
Она говорит о том, что витамин В9 и витамин В12, вообще не усваиваются организмом. То есть усвояемость, если повезет 0-15%, при моей мутации. Особенно В12 не усваивается.
Многие думают, что данная мутация в первую очередь влияет на гомоцистеин, ничего подобного (то есть она влияет, но не в этом проблема этой мутации). По моим анализам видно, что он в норме, а витамины группы В все равно не усваиваются и мне плохо от них, организм их просто отторгает в неизменном виде.
Если в организме не достаточно фолиевой и В12, то начинаются генетические нарушения уже во время деления яйцеклетки, то есть она уже с отклонениями, когда начинает делиться. При этой мутации очень часты генетические проблемы плода, особенно дауны и болезни нервной трубки и иные заболевания головного мозга. Поэтому матка генетически нездоровую оплодотворенную яйцеклетку будет отторгать.
Если у вас есть мутации в фолатном цикле, покупаем витамины, даже если у вас нормальный гомоцистеин их надо пить!!!! в поддерживающей дозировке и не ангиовит или фолю в ядерной дозировке, если у вас гомозигота вам не поможет.
Метилфолат – фолька
Метилкобаламин – В12 (этот витамин на 1 месте стоит именно при этой мутации и именно фолаты.
пиродоксаль-фосфат – еще инет рекомендует при этой мутации добавить витамин В6 в усвояемой форме – по желанию (от какого-то доктора по генетике нашла что он при этой мутации рекомендует связку В6+В12+В9 иначе страдает генетика у плода.
Вспомнила: долго не могла забеременеть сыном, 2,5 года у нас с мужем не получалось при стабильном цикле, врач грешила на спайки. Я тогда думала, что мне помог электрофорез (наивная). Но мне врач в этот же цикл назначила фольку и витамин Е. А перед этим я прошла курс уколов Алоэ+В1+В6+В12. Это видно и запустило у меня процесс зачатия в нужное русло. И у нас все получилось. Причем одна фолька мне не помогает.
2. Проблема
Нашла одно аутоиммунное заболевание (по АНФ). Если есть одно, есть и другие. Это собственный иммунитет убивает клетки. Тем более АСАТ пришел 17, то есть есть антитела к сперме. Знаю, что девочки легко беременеют и вынашивают при АСАТ ноль, а если он не ноль начинаются проблемы.
Тут вам не подскажу, знаю, что используют для ослабления антител метипред, ИГ, ПФ. Это надо к спецу, которого не так легко найти.
Тут я буду еще досдавать: АТ к ТПО, АТ к ХГЧ, иммуноглобулина А, М, G, Е. Если они подтвердятся придется плазмафорез делать и ИГ.
Так же аутоиммунные заболевания вызывают эндометриоз. Как раз прям про меня.
Еще буду проверять на целиакию (это аллергия на глютен) и аллергены к продуктам питания – это они подстегивают все аутоиммунные болячки. Тем более у меня проблемы с пищеварением.
***
Начну с витаминов и диеты.
Нужно 3 месяца, чтобы накопилось в клетках нужное количество витаминов в яичниках. И аутоиммуннка ослабла. Но со 2 проблемой сложнее бороться. Пока там низкие титры, но они есть.
И надеюсь у нас скоро все получится
****
АНАЛИЗЫ
Так как много народу спрашивает, что проверить, пишу сюда:
1. Генетика на мутации
Сюда входят:
• F2 c.*97G>A (20210 G>A; rs1799963),
• F5 c.1601G>A (Arg534Gln; 1691 G>A; rs6025),
• MTHFR c.665C>T (Ala222Val; 677 C>T; rs1801133),
• MTHFR c.1286A>C (Glu429Ala; 1298 A>C; rs1801131),
• MTR c.2756A>G (Asp919Gly; rs1805087),
• MTRR c.66A>G (Ile22Met; rs1801394),
• F13 с.103G>T (I63Т; rs5985),
• FGB c.-467G>A (-455 G>А; rs1800790),
• ITGA2 c.759C>T (Phe253Phe, 807 C>T; rs1126643),
• ITGB3 c.176T>C (Leu59Pro; 1565 T>C; rs5918),
• F7 c.1238G>A (Arg353Gln; 10976 G>A; rs6046),
• PAI-1 (SERPINE1) -675 5G>4G (rs1799889).
2. АФС синдром
Сюда входят:
Антитела к кардиолипину IgG
Антинуклеарный фактор (АНФ)
Антитела к бета-2-гликопротеину 1, суммарные IgG, IgA, IgM
Антитела к кардиолипину, IgM
3. АТ к ТПО – аутоиммунка
4. АСАТ (антисперальные для женщин – кровь)
5. Гомоцистеин
6. Гемостаз
В него входит:
Протромбин (протромбиновое время, протромбин (по Квику), МНО – международное нормализованное отношение),
АЧТВ (активированное частичное тромбопластиновое время)
Фибриноген
Тромбиновое время
Антитромбин III
Д-димер
Плазминоген
Волчаночный антикоагулянт
Это то что надо обязательно всем проверить, если долго не получается.
Если у вас найдут антитела к чему-либо, то это может говорить об аутоиммунном процессе, ваша собственная иммунная система очень агрессивно настроена на процессы в организме.
ссылки даны на Инвитро, но вы все это можете сдать в любой лаборатории, просто у нас она в городе единственная.
Источник
