Как называется цикл реакций связанных с дегидрированием

Представьте себе, что все белки, жиры и углеводы, которые мы получаем с приемом пищи, распадаются на маленькие пазлы, которые собираются вновь только в одном определенном участке нашего организма – митохондриях. Там же происходит сортировка и параллельное протекание реакций созидания и разрушения. Разберемся подробнее:
Что такое цикл Кребса
Цикл Кребса – это цепочка химических реакций, происходящих в митохондриях каждой клетки нашего тела, которая называется циклом потому, что продолжается непрерывно. Она же является и общим конечным путем окисления ацетильных групп (в виде ацетил-КоА), в которые превращается в процессе распада большая часть органических молекул, играющих роль «клеточного топлива» или «субстратов окисления»: углеводов, жирных кислот и аминокислот.
Функции цикла Кребса:
- анаболическая (синтез новых органических веществ);
- энергетическая (питание организма)
- катаболическая (превращение некоторых веществ в катализаторы)
- транспортная (транспортировка водорода, участвующего в дыхании клеток).
Атомы водорода, высвобождающиеся в окислительно-восстановительных реакциях, доставляются в цепь переноса электронов при участии НАД- и ФАД- зависимых дегидрогеназ, в результате чего происходит образование 12 высокоэнергетических фосфатных связей: синтез 12 молекул аденозинтрифосфорной кислоты (АТФ) из аденозиндифосфорной кислоты (АДФ).
Как работает цикл Кребса?
В организме аминокислоты, жирные кислоты и пируват образуют ацетил-КоА.
Когда ацетил-КоА попадает в митохондриальный матрикс, он связывается с молекулой оксалацетата и превращается в лимонную кислоту (цитрат). Цитрат, в свою очередь, под действием фермента аконитазы превращается в цис-аконитат, оставляя молекулу воды.
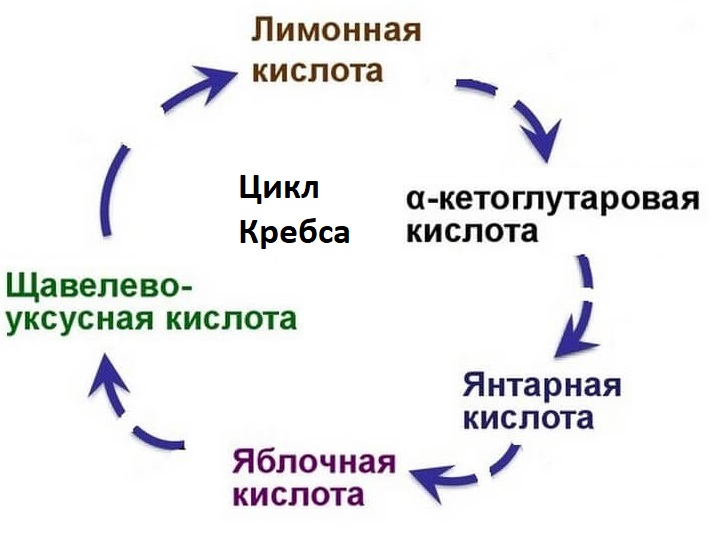
В свою очередь цис-аконитат превращается в изоцитрат под действием фермента изоцитратдегидрогеназы. Изоцитрат превращается в альфа-кетоглутарат под действием изоцитратдегидрогеназы.
Альфа-кетоглутарат превращается в сукцинил-КоА альфа-кетоглутаратдегидрогеназой и добавлением ацетил-КоА. Он подвергается сукцинату под действием сукцинат-тиокиназы. Сукцинатдегидрогеназа превращает его в фумарат. Фумарат превращается в L-малат через фумаразу. L-малат под действием фермента малатдегидрогеназы восстанавливает оксалацетат, который может снова вступать в реакцию с молекулой ацетил-КоА и повторять цикл.
Результатом этого цикла является образование CO2 и водорода, а также воды. Ионы на выходе из процесса участвуют в ресинтезе АТФ, что помогает организму восстановить еще один источник энергии – трифосфат аденозина.
Стадии цикла Кребса
Окисление ацетильного остатка происходит в несколько стадий, образующих циклический процесс из 8 основных этапов:
Основные этапы цикла Кребса | |
I этап | Конденсация ацетил-КоА и оксалоацетата с образованием цитрата. |
Происходит реакция отщепление карбоксильной группы аминокислот, в процессе которой образуется ацетил-КоА *он выполняет функцию транспортировки углерода в различных обменных процессах. При соединении с молекулой щавелевой кислоты получается цитрат *фигурирует в буферных обменах. На данном этапе кофермент А полностью высвобождается, и получаем молекулу воды. Данная реакция необратима. | |
II этап | Превращение цитрата в изоцитрат. |
Дегидрирование (отщепление молекул воды) от цитрата, в результате которого получается цис-аконитат. И присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат) | |
III этап | Превращение изоцитрата в а-кетоглутарат. |
Изолимонная кислота(изоцитрат) дегидрируется в присутствии НАД- зависимой изо-цитратдегидрогеназы.На выходе получаем альфа-кетоглутарат. *Альфа-кетоглутарат участвует в регуляции всасывания аминокислот, нормализует метаболизм и положительно влияет на антистрессорные процессы. Также образуется NADH (аллостерический фермент) | |
IV этап | Окисление α-кетоглутарата до сукцинил-КоА |
Окислительное декарбоксилирование а-кетоглутарата с образованием сукцинил-КоА – тиоэфира, содержащего высокоэнергетическую фосфатную связь. | |
V этап | Превращение сукцинил-КоА в сукцинат. |
Пятая реакция катализируется ферментом сукцинил-КоА-синтетазой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Так же происходит образование высокоэргической фосфатной связи ГТФ за счет тиоэфирной связи сукцинил-КоА. | |
VI этап | Дегидрогенирование сукцината. Образование фумарата. |
Образовавшийся сукцинат превращается в фумарат под действием фермента сукцинат-дегидрогеназы. Единственная дегидрогеназная реакция цикла Кребса, в ходе которой осуществляется прямой перенос водорода с субстрата на флавопротеин без участия НАД+. | |
VII этап | Образование малата из фумарата. |
Под влиянием фермента фумаратгидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является L-яблочная кислота (L-малат). | |
VIII этап | Превращение малата в оксалоацетат. |
Под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат. Происходит полное «сгорание» одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА. А коферменты (НАД+ и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться. | |
Реакции цикла Кребса по стадиям
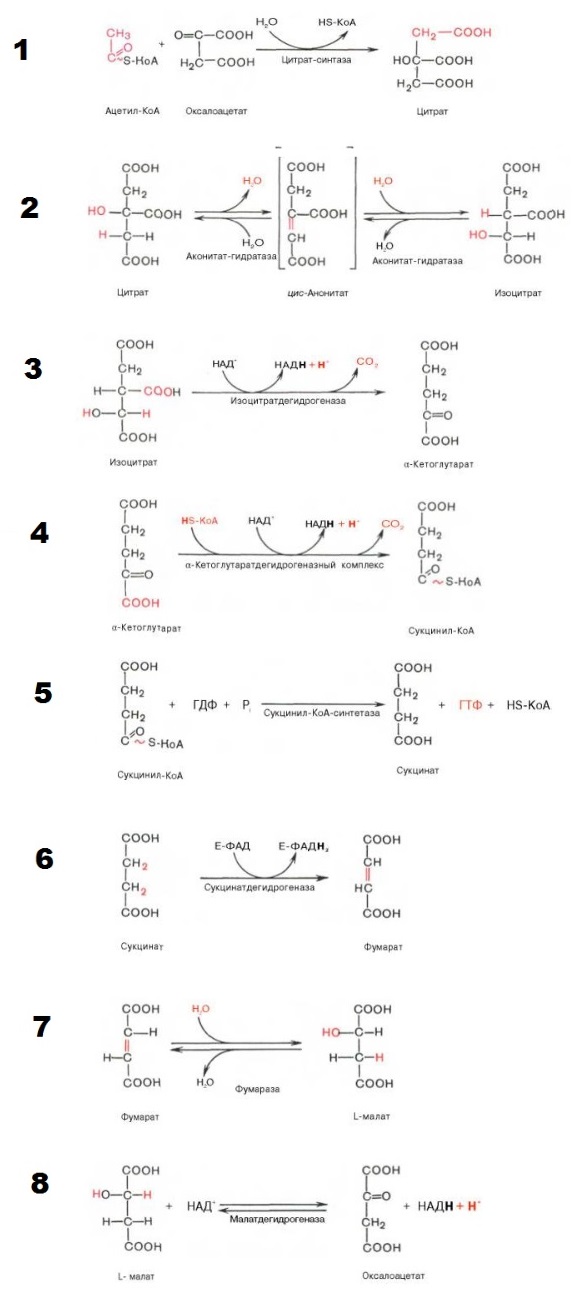
Для облегчения запоминания ферментативных реакций цикла:
ЩУКа съела ацетат, получается цитрат
через цис-аконитат будет он изоцитрат
водороды отдав НАД, он теряет СО2
этому безмерно рад альфа-кетоглутарат
окисление грядёт: НАД похитит водород
В1 и липоат с коэнзимом А спешат,
отбирают СО2, а энергия едва
в сукциниле появилась сразу ГТФ родилась
и остался сукцинат. вот добрался он до ФАДа,
водороды тому надо водороды потеряв,
стал он просто фумарат. фумарат воды напился,
и в малат он превратился тут к малату НАД пришёл,
водороды приобрёл ЩУКа снова объявилась
и тихонько затаилась Караулить ацетат…
Источник
1
H
1,008
1s1
2,1
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
4,5
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
3,98
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
4,4
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,98
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
4,3
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Источник
Реагент и субстрат
Существуют разные системы классификации органических реакций, которые основаны на различных признаках. Среди них можно выделить классификации:
по конечному результату реакции, то есть изменению в структуре субстрата;
по механизму протекания реакции, то есть по типу разрыва связей и типу реагентов.
Взаимодействующие в органической реакции вещества подразделяют на реагент и субстрат. При этом считается, что реагент атакует субстрат.
Определение
Реагент — вещество, действующее на объект — субстрат — и вызывающее в нем изменение химической связи. Реагенты делятся на радикальные, электрофильные и нуклеофильные.
Определение
Субстратом, как правило, считают молекулу, которая предоставляет атом углерода для новой связи.
КЛАССИФИКАЦИЯ РЕАКЦИЙ ПО КОНЕЧНОМУ РЕЗУЛЬТАТУ (ИЗМЕНЕНИЮ В СТРУКТУРЕ СУБСТРАТА)
В органической химии различают четыре вида реакций по конечному результату и изменению в структуре субстрата: присоединения, замещения, отщепления, или элиминирования (от англ. to eliminate — удалять, отщеплять), и перегруппировки (изомеризации). Такая классификация аналогична классификации реакций в неорганической химии по числу исходных реагентов и образующихся веществ, с изменением или без изменения состава. Классификация по конечному результату основана на формальных признаках, так как стехиометрическое уравнение, как правило, не отражает механизм реакции. Сравним типы реакций в неорганической и органической химии.
Тип реакции в неорганической химии | Пример | Тип реакции в органической химии | Разновидность и пример реакции |
|---|---|---|---|
1. Соединение | $Cl_2+H_2 = 2HCl$ | Присоединение по кратным связям | Гидрирование
|
Гидрогалогенирование
| |||
Галогенирование
| |||
Гидратация
| |||
2. Разложение | $2H_2O = 2H_2+O_2$ | Элиминирование | Дегидрирование
|
Дегидрогалогенирование
| |||
Дегалогенирование
| |||
Дегидратация
| |||
3. Замещение | $Zn+2HCl =$ $ZnCl_2+H_2$ | Замещение |
|
4. Обмен (частный случай — нейтрализация) | $H_2SO_4+2NaOH$ = $Na_2SO_4+2H_2O$ | частный случай — этерификация |
|
5.Аллотропизация | графит$ Leftrightarrow$ алмаз $P_{textrm{красн.}} Leftrightarrow P_{textrm{ бел.}}$ $S_{textrm{ромб.}} Leftrightarrow S _{textrm{пласт.}}$ | Изомеризация | Изомеризация алканов
|
Определение
Элиминирование — отщепление от молекулы органических соединений частиц (атомов или атомных групп) без замены их другими.
В зависимости от того, какие атомы отщепляются — соседние C–C или изолированные двумя-тремя или более атомами углерода –C–C–C–C–, –C–C–C–C–C–, могут образовываться соединения с кратными связями или циклические соединения. Отщепление галогеноводородов из алкилгалогенидов либо воды из спиртов происходит по правилу Зайцева.
Определение
Правило Зайцева: атом водорода Н отщепляется от наименее гидрогенизированного атома углерода.
Например, отщепление молекулы бромоводорода происходит от соседних атомов в присутствии щелочи, при этом образуется бромид натрия и вода.

Определение
Перегруппировка — химическая реакция, в результате которой происходит изменение взаимного расположения атомов в молекуле, перемещение кратных связей или изменение их кратности.
Перегруппировка может осуществляться с сохранением атомного состава молекулы (изомеризация) или с его изменением.
Определение
Изомеризация — частный случай реакции перегруппировки, приводящая к превращению химического соединения в изомер путем структурного изменения углеродного скелета.
Перегруппировка тоже может осуществляться по гомолитическому или гетеролитическому механизму. Молекулярные перегруппировки могут классифицироваться по разным признакам, например по насыщенности систем, по природе мигрирующей группы, по стереоспецифичности и др. Многие реакции перегруппировки имеют специфические названия — перегруппировка Кляйзена, перегруппировка Бекмана и др.
Реакции изомеризации широко используются в промышленных процессах, например при переработке нефти для повышения октанового числа бензина. Примером изомеризации является превращение н-октана в изооктан:

КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ ПО ТИПУ РЕАГЕНТА
РАЗРЫВ СВЯЗИ
Разрыв связи в органических соединениях может гомолитическим и гетеролитическим.
Определение
Гомолитический разрыв связи — это такой разрыв, в результате которого каждый атом получает неспаренный электрон и образуются две частицы, имеющие сходное электронное строение — свободные радикалы.
Гомолитический разрыв характерен для неполярных или слабополярных связей, например C–C, Cl–Cl, C–H, и требует большого количества энергии.
Образующиеся радикалы, имеющие неспаренный электрон, обладают высокой реакционной способностью, поэтому химические процессы, протекающие с участием таких частиц, часто носят «цепной» характер, их трудно контролировать, а в результате реакции получается набор продуктов замещения. Так, при хлорировании метана продуктами замещения являются хлорметан $CH_3Cl$, дихлорметан $CH_2Cl_2$, хлороформ $CHCl_3$ и четыреххлористый углерод $CCl_4$. Реакции с участием свободных радикалов протекают по обменному механизму образования химических связей.
Образующиеся в ходе такого разрыва связи радикалы обуславливают радикальный механизм протекания реакции. Радикальные реакции обычно протекают при повышенных температурах или при излучении (например, свет).
В силу своей высокой реакционной способности свободные радикалы могут оказывать негативное воздействие на организм человека, разрушая клеточные мембраны, воздействуя на ДНК и вызывая преждевременное старение. Эти процессы связаны, в первую очередь, с пероксидным окислением липидов, то есть разрушением структуры полиненасыщенных кислот, образующих жир внутри клеточной мембраны.
Определение
Гетеролитический разрыв связи — это такой разрыв, при котором электронная пара остается у более электроотрицательного атома и образуются две заряженные частицы — ионы: катион (положительный) и анион (отрицательный).
В химических реакциях эти частицы выполняют функции «нуклеофилов» («фил» — от гр. любить) и «электрофилов», образуя химическую связь с партнером по реакции по донорно-акцепторному механизму. Частицы-нуклеофилы предоставляют электронную пару для образования новой связи. Другими словами,
Определение
Нуклеофил — электроноизбыточный химический реагент, способный взаимодействовать с электронодефицитными соединениями.
Примерами нуклеофилов являются любые анионы ($Cl^-, I^-, NO_3^-$ и др.), а также соединения, имеющие неподеленную электронную пару ($NH_3, H_2O$).
Таким образом, при разрыве связи могут образоваться радикалы или нуклеофилы и электрофилы. Исходя из этого выделяют три механизма протекания органических реакций.
МЕХАНИЗМЫ ПРОТЕКАНИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
Свободно-радикальный механизм: реакцию начинают свободные радикалы, образующиеся при гомолитическом разрыве связи в молекуле.
Наиболее типичный вариант — образование радикалов хлора или брома при УФ-облучении.
1. Свободно-радикальное замещение


метан $hspace {10 cm}$ бромметан
Инициирование цепи

Рост цепи

Обрыв цепи

2. Свободно-радикальное присоединение

этен $hspace{14 cm}$ полиэтилен
Электрофильный механизм: реакцию начинают частицы-электрофилы, получающие положительный заряд в результате гетеролитического разрыва связи. Все электрофилы — кислоты Льюиса.
Такие частицы активно образуются под действием кислот Льюиса, которые усиливают положительный заряд частицы. Чаще других используются $AlCl_3, FeCl_3, FeBr_3, ZnCl_2$, выполняющие функции катализатора.
Местом атаки частицы-электрофила являются те участки молекулы, которые имеют повышенную электронную плотность, т. е. кратная связь и бензольное кольцо.
Общий вид реакций электрофильного замещения можно выразить уравнением:
1. Электрофильное замещение

бензол $hspace{14 cm}$ бромбензол
2. Электрофильное присоединение

пропен $hspace {23 cm}$2-бромпропан

пропин $hspace {20 cm}$1,2-дихлорпропен
Присоединение к несимметричным непредельным углеводородам происходит в соответствии с правилом Марковникова.
Определение
Правило Марковникова: присоединение к несимметричным алкенам молекул сложных веществ с условной формулой НХ (где Х — это атом галогена или гидроксильная группа ОН–) атом водорода присоединяется к наиболее гидрогенизированному (содержащему больше всего атомов водорода) атому углерода при двойной связи, а Х — к наименее гидрогенизированному.
Например, присоединение хлороводорода HCl к молекуле пропена $CH_3–CH=CH_2$.

Реакция протекает по механизму электрофильного присоединения. За счет электронодонорного влияния $CH_3$-группы электронная плотность в молекуле субстрата смещена к центральному атому углерода (индуктивный эффект), а затем по системе двойных связей — к концевому атому углерода $CH_2$-группы (мезомерный эффект). Таким образом, избыточный отрицательный заряд локализован именно на этом атоме. Поэтому атаку начинает протон водорода $H^+$, являющийся электрофильной частицей. Образуется положительно заряженный карбеновый ион $[CH_3–CH-CH_3]^+$, к которому присоединяется анион хлора $Cl^-$.
Определение
Исключения из правила Марковникова: реакция присоединения протекает против правила Марковникова, если в реакцию вступают соединения, у которых атом углерода, соседний с атомом углерода двойной связи, оттягивает на себя частично электронную плотность, то есть при наличии заместителей, проявляющих значительный электроноакцепторный эффект $(–CCl_3, –CN, –COOH$ и др.).

Нуклеофильный механизм: реакцию начинают частицы-нуклеофилы, имеющие отрицательный заряд, образовавшиеся в результате гетеролитического разрыва связи. Все нуклеофилы — основания Льюиса.
В нуклеофильных реакциях реагент (нуклеофил) имеет на одном из атомов свободную пару электронов и является нейтральной молекулой или анионом ($Hal^–, OH^–, RO^-, RS^–, RCOO^–, R^–, CN–, H_2O, ROH, NH_3, RNH_2$ и др.).
Нуклеофил атакует в субстрате атом с наименьшей электронной плотностью (т. е. с частичным или полным положительным зарядом). Первой стадией реакции нуклеофильного замещения является ионизация субстрата с образованием карбкатиона. При этом новая связь образуется за счет электронной пары нуклеофила, а старая претерпевает гетеролитический разрыв с последующим отщеплением катиона. Примером нуклеофильной реакции может служить нуклеофильное замещение (символ $S_N$) у насыщенного атома углерода, например щелочной гидролиз бромпроизводных.
1. Нуклеофильное замещение

2. Нуклеофильное присоединение

этаналь $hspace{13 cm}$ циангидрин
Задача
Написать уравнения реакций в соответствии со схемой превращений, указать продукты, тип реакций и механизмы:
$CH_3–CH_3 hspace{0.7cm} xrightarrow[]{1} hspace{0.7cm} CH_3–CH_2Clhspace{0.7cm} xrightarrow[]{2} hspace{0.7cm} CH_2=CH_2 hspace{0.7cm} xrightarrow[]{3} hspace{0.7cm} CH_3–CH_2–OH$
1. Определим классы, к которым принадлежат вещества в схеме. и назовем их.
Данная схема отражает следующую цепочку превращений: алкан (этан) $ hspace{0.2cm} xrightarrow[]{1} hspace{0.2cm}$ монохлорзамещенный алкан (хлорэтан) $ hspace{0.2cm} xrightarrow[]{2} hspace{0.2cm}$ алкен (этен) $ hspace{0.2cm} xrightarrow[]{3} hspace{0.2cm}$ одноатомный предельный спирт (этанол).
2. Определим типы и разновидности реакций по конечному продукту:
1) реакция замещения — галогенирование;
2) реакция элиминирования — дегидрохлорирование;
3) реакция присоединения — гидратация.
3. Определим возможные механизмы реакций, вспомним условия их проведения и запишем уравнения реакций:
1) хлорирование предельных УВ протекает по свободно-радикальному механизму, условия — УФ-облучение:
$Cl_2 longrightarrow Cl cdot + cdot Cl$;
$CH_3–CH_3 +cdot Cl longrightarrow CH_3–CH_2cdot + HCL$
$CH_3–CH_2 cdot + cdot C longrightarrow CH_3–CH_2Cl$.
2) в присутствии основания NaOH реакция протекает по карбанионному механизму:

Сначала в щелочной среде отщепляется протон водорода Н, а затем анион галогена X. Это двухстадийный процесс, в котором промежуточным продуктом является карбанион. Условие реакции — спиртовой раствор щелочи NaOH.
3) гидратация непредельных УВ протекает по механизму электрофильного присоединения:

Условием проведения реакции является кислая среда, поэтому реакцию проводят в присутствии серной кислоты $H_2SO_4 $.









