Альфа кетоглутарат в цикле кребса
| Альфа-кетоглутаровая кислота | |
|---|---|
| Систематическое наименование | 2-оксопентандиовая кислота |
| Традиционные названия | α-кетоглутаровая кислота, 2-оксоглутаровая кислота |
| Хим. формула | C5H6O5 |
| Состояние | твёрдое |
| Молярная масса | 146,0981 ± 0,0059 г/моль |
| Температура | |
| • плавления | 112-116 °C |
| • кипения | 160 °C |
| Растворимость | |
| • в воде | 10 г/100 мл |
| Рег. номер CAS | 328-50-7 |
| PubChem | 51 |
| Рег. номер EINECS | 206-330-3 |
| SMILES | O=C(O)C(=O)CCC(=O)O |
| InChI | InChI=1S/C5H6O5/c6-3(5(9)10)1-2-4(7)8/h1-2H2,(H,7,8)(H,9,10) KPGXRSRHYNQIFN-UHFFFAOYSA-N |
| ChEBI | 30915 |
| ChemSpider | 50 |
| Токсичность | едкое вещество, сильно раздражает кожу, является ирритантом |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
| Медиафайлы на Викискладе | |
α-Кетоглутаровая (альфа-кетоглутаровая) кислота – одно из двух кетоновых производных глутаровой кислоты. Название «кетоглутаровая кислота» без дополнительных обозначений обычно означает альфа-форму. Отличается от β-кетоглутаровой кислоты только положением кетонной функциональной группы и встречается гораздо реже[1].
Анион α-кетоглутаровой кислоты, α-кетоглутарат (также называемый оксоглутарат) – важное биологическое соединение. Это кетокислота, которая образуется при дезаминировании глутамата. α-Кетоглутарат является одним из соединений, образующихся в цикле Кребса.[1][2]
Биологическое значение[править | править код]
Цикл Кребса[править | править код]
α-Кетоглутарат – ключевой продукт цикла трикарбоновых кислот , образуется в результате декарбоксилирования изоцитрата и превращается в сукцинил-CoA в альфа-кетоглутарат дегидрогеназном комплексе. Анаплеротические реакции могут пополнять цикл на данном этапе путём синтеза α-кетоглутарата трансаминированием глутамата, или действием глутаматдегидрогеназы на глутамат.[2]
Синтез аминокислот[править | править код]
Глутамин синтезируется из глутамата с помощью фермента глутаминсинтетазы, которая на первой стадии образует глутамилфосфат, используя в качестве донора фосфата АТФ; глутамин образуется в результате нуклеофильного замещения фосфата катионом аммония в глутамилфосфате, продуктами реакции являются глутамин и неорганический фосфат.[2]
Транспорт аммиака[править | править код]
Другой функцией альфа-кетоглутаровой кислоты является транспорт аммиака, выделяющегося в результате катаболизма аминокислот.[2]
α-Кетоглутарат – один из важнейших переносчиков аммиака в метаболических путях. Аминогруппы от аминокислот прикрепляются к α-кетоглутарату в реакции трансаминирования и переносятся в печень, попадая в цикл мочевины.[3]
Продление жизни[править | править код]
Обнаружено, что α-кетоглутарат, благодаря его способности подавлять АТФ-синтазу и таким образом понижать уровень АТФ, а также ингибировать mTOR, способен увеличивать продолжительности жизни нематод[4], мухи Drosophila[5] и мыши[6]
Примечания[править | править код]
- ↑ 1 2 Биохимия. Краткий курс с упражнениями и задачами / Под ред. Е. С. Северина и А. Я. Николаева. – М.: ГЭОТАР-МЕД, 2001. – 448 с., ил.
- ↑ 1 2 3 4 Филиппович Ю. Б. Основы биохимии: Учеб. для хим. и биол. спец. пед. ун-тов и ин-тов / Ю. Б. Филиппович. – 4-е изд., перераб. и доп. – М.: «Агар», 1999. – 512 с., ил.
- ↑ Березов Т. Т. Биологическая химия: Учебник / Т. Т. Березов, Б. Ф. Коровкин. – 3-е изд., перераб. и доп. – М.: Медицина, 1998. – 704 с., ил.
- ↑ Chin, R. M., Fu, X., Pai, M. Y., Vergnes, L., Hwang, H., Deng, G., … & Hu, E. (2014). The bolite α-ketoglutarate extends lifespan by inhibiting ATP synthase and TOR. Nature, 510(7505), 397-401. doi:10.1038/nature13264 PMC 4263271 PMID 24828042
- ↑ Su, Y., Wang, T., Wu, N., Li, D., Fan, X., Xu, Z., … & Yang, M. (2019). Alpha-ketoglutarate extends Drosophila lifespan by inhibiting mTOR and activating AMPK. Aging (Albany NY), 11(12), 4183. doi:10.18632/aging.102045 PMC 6629006 PMID 31242135
- ↑ Shahmirzadi, A. A., Edgar, D., Liao, C. Y., Hsu, Y. M., Lucanic, M., Shahmirzadi, A. A., … & Kuehnemann, C. (2020). Alpha-ketoglutarate, an endogenous bolite, extends lifespan and compresses morbidity in aging mice. Cell bolism, 32(3), 447-456.e6 doi:10.1016/j.cmet.2020.08.004 PMID 32877690
Источник
Представьте себе, что все белки, жиры и углеводы, которые мы получаем с приемом пищи, распадаются на маленькие пазлы, которые собираются вновь только в одном определенном участке нашего организма – митохондриях. Там же происходит сортировка и параллельное протекание реакций созидания и разрушения. Разберемся подробнее:
Что такое цикл Кребса
Цикл Кребса – это цепочка химических реакций, происходящих в митохондриях каждой клетки нашего тела, которая называется циклом потому, что продолжается непрерывно. Она же является и общим конечным путем окисления ацетильных групп (в виде ацетил-КоА), в которые превращается в процессе распада большая часть органических молекул, играющих роль «клеточного топлива» или «субстратов окисления»: углеводов, жирных кислот и аминокислот.
Функции цикла Кребса:
- анаболическая (синтез новых органических веществ);
- энергетическая (питание организма)
- катаболическая (превращение некоторых веществ в катализаторы)
- транспортная (транспортировка водорода, участвующего в дыхании клеток).
Атомы водорода, высвобождающиеся в окислительно-восстановительных реакциях, доставляются в цепь переноса электронов при участии НАД- и ФАД- зависимых дегидрогеназ, в результате чего происходит образование 12 высокоэнергетических фосфатных связей: синтез 12 молекул аденозинтрифосфорной кислоты (АТФ) из аденозиндифосфорной кислоты (АДФ).
Как работает цикл Кребса?
В организме аминокислоты, жирные кислоты и пируват образуют ацетил-КоА.
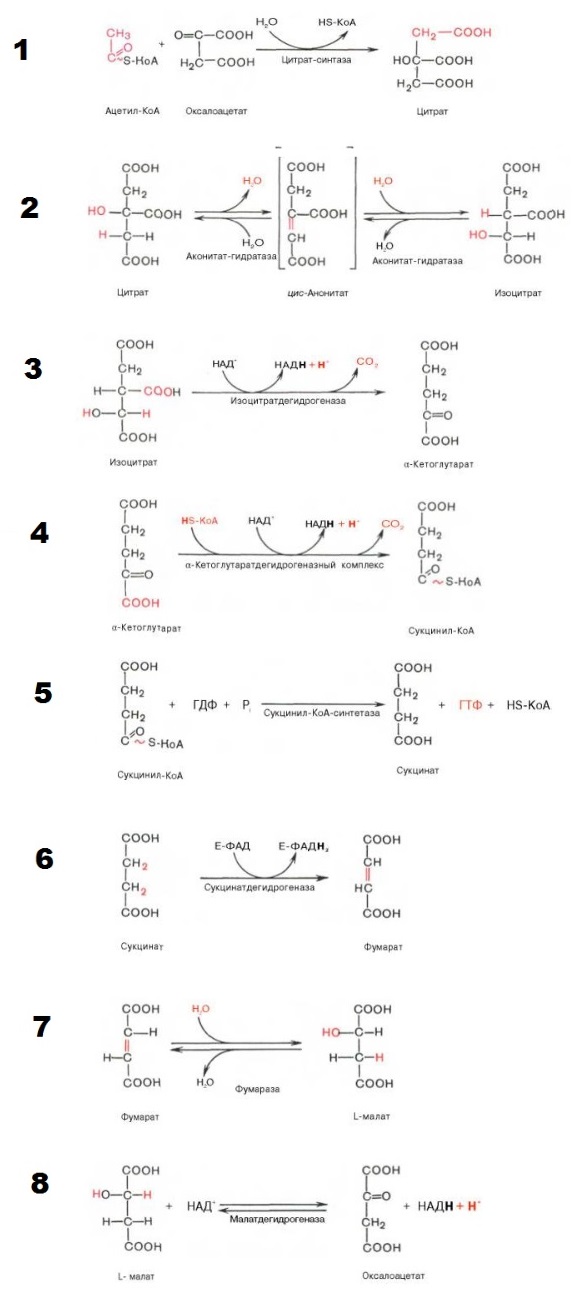
Когда ацетил-КоА попадает в митохондриальный матрикс, он связывается с молекулой оксалацетата и превращается в лимонную кислоту (цитрат). Цитрат, в свою очередь, под действием фермента аконитазы превращается в цис-аконитат, оставляя молекулу воды.
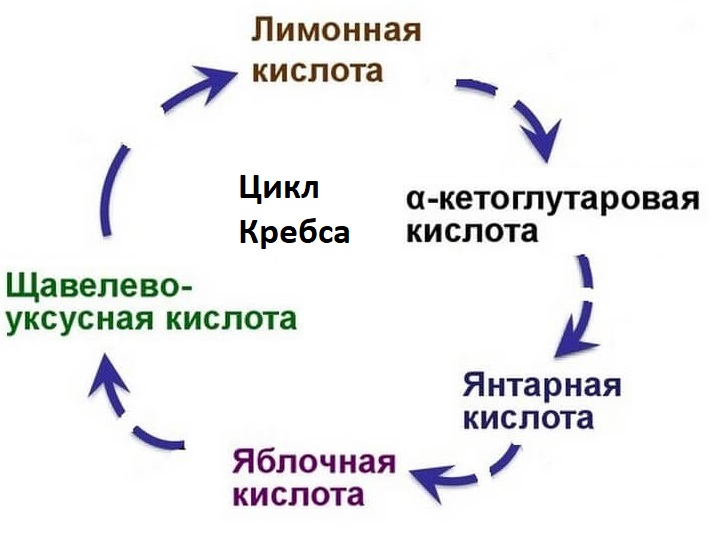
В свою очередь цис-аконитат превращается в изоцитрат под действием фермента изоцитратдегидрогеназы. Изоцитрат превращается в альфа-кетоглутарат под действием изоцитратдегидрогеназы.
Альфа-кетоглутарат превращается в сукцинил-КоА альфа-кетоглутаратдегидрогеназой и добавлением ацетил-КоА. Он подвергается сукцинату под действием сукцинат-тиокиназы. Сукцинатдегидрогеназа превращает его в фумарат. Фумарат превращается в L-малат через фумаразу. L-малат под действием фермента малатдегидрогеназы восстанавливает оксалацетат, который может снова вступать в реакцию с молекулой ацетил-КоА и повторять цикл.
Результатом этого цикла является образование CO2 и водорода, а также воды. Ионы на выходе из процесса участвуют в ресинтезе АТФ, что помогает организму восстановить еще один источник энергии – трифосфат аденозина.
Стадии цикла Кребса
Окисление ацетильного остатка происходит в несколько стадий, образующих циклический процесс из 8 основных этапов:
Основные этапы цикла Кребса | |
I этап | Конденсация ацетил-КоА и оксалоацетата с образованием цитрата. |
Происходит реакция отщепление карбоксильной группы аминокислот, в процессе которой образуется ацетил-КоА *он выполняет функцию транспортировки углерода в различных обменных процессах. При соединении с молекулой щавелевой кислоты получается цитрат *фигурирует в буферных обменах. На данном этапе кофермент А полностью высвобождается, и получаем молекулу воды. Данная реакция необратима. | |
II этап | Превращение цитрата в изоцитрат. |
Дегидрирование (отщепление молекул воды) от цитрата, в результате которого получается цис-аконитат. И присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат) | |
III этап | Превращение изоцитрата в а-кетоглутарат. |
Изолимонная кислота(изоцитрат) дегидрируется в присутствии НАД- зависимой изо-цитратдегидрогеназы.На выходе получаем альфа-кетоглутарат. *Альфа-кетоглутарат участвует в регуляции всасывания аминокислот, нормализует метаболизм и положительно влияет на антистрессорные процессы. Также образуется NADH (аллостерический фермент) | |
IV этап | Окисление α-кетоглутарата до сукцинил-КоА |
Окислительное декарбоксилирование а-кетоглутарата с образованием сукцинил-КоА – тиоэфира, содержащего высокоэнергетическую фосфатную связь. | |
V этап | Превращение сукцинил-КоА в сукцинат. |
Пятая реакция катализируется ферментом сукцинил-КоА-синтетазой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Так же происходит образование высокоэргической фосфатной связи ГТФ за счет тиоэфирной связи сукцинил-КоА. | |
VI этап | Дегидрогенирование сукцината. Образование фумарата. |
Образовавшийся сукцинат превращается в фумарат под действием фермента сукцинат-дегидрогеназы. Единственная дегидрогеназная реакция цикла Кребса, в ходе которой осуществляется прямой перенос водорода с субстрата на флавопротеин без участия НАД+. | |
VII этап | Образование малата из фумарата. |
Под влиянием фермента фумаратгидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является L-яблочная кислота (L-малат). | |
VIII этап | Превращение малата в оксалоацетат. |
Под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат. Происходит полное «сгорание» одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА. А коферменты (НАД+ и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться. | |
Реакции цикла Кребса по стадиям

Для облегчения запоминания ферментативных реакций цикла:
ЩУКа съела ацетат, получается цитрат
через цис-аконитат будет он изоцитрат
водороды отдав НАД, он теряет СО2
этому безмерно рад альфа-кетоглутарат
окисление грядёт: НАД похитит водород
В1 и липоат с коэнзимом А спешат,
отбирают СО2, а энергия едва
в сукциниле появилась сразу ГТФ родилась
и остался сукцинат. вот добрался он до ФАДа,
водороды тому надо водороды потеряв,
стал он просто фумарат. фумарат воды напился,
и в малат он превратился тут к малату НАД пришёл,
водороды приобрёл ЩУКа снова объявилась
и тихонько затаилась Караулить ацетат…
Источник
| Имена | |
|---|---|
| Предпочтительное название IUPAC 2-оксопентандиовая кислота | |
| Другое наименования 2-кетоглутаровая кислота альфа-кетоглутаровая кислота 2-оксоглутаровая кислота оксоглутаровая кислота | |
| Идентификаторы | |
Номер CAS |
|
3D-модель ( JSmol ) |
|
| ChEBI |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA Card | 100.005.756 |
IUPHAR / BPS |
|
| KEGG |
|
| MeSH | альфа-кетоглутаровая + кислота |
PubChem CID |
|
| UNII |
|
CompTox Dashboard ( EPA ) |
|
InChI
| |
УЛЫБКА
| |
| Свойства | |
Химическая формула | C5H6O5 |
| Молярная масса | 146,11 г / моль |
| Температура плавления | 115 ° С (239 ° F; 388 K) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| N (what является ?) | |
| Ссылки на box | |
α-Кетоглутаровая кислота (2-оксоглутаровая кислота ) является одним из двух кетонов производных глутаровой кислоты. кислота . Термин «кетоглутаровая кислота», если он не уточняется, почти всегда относится к альфа-варианту. β-Кетоглутаровая кислота варьируется только положением кетонафункциональной группы и встречается гораздо реже.
Его анион , α-кетоглутарат , также называемый 2-оксоглутарат , является важным биологическим соединением. Это кетокислота , продуцируемая дезаминированием глутамата , и является промежуточным звеном в цикле Кребса .
Функции
Аланинтрансаминаза
Фермент аланинтрансаминаза превращает α-кетоглутарат и L-аланин в L-глутамат и пируват соответственно в качестве обратимого процесса.
Цикл Кребса
α-Кетоглутарат является ключевым промежуточным продуктом в цикле Кребса , идущим после изоцитрата и до сукцинил-КоА . Анаплеротические реакции могут восполнить цикл на этом этапе путем синтеза α-кетоглутарата путем трансаминирования глутамата или посредством действия глутаматдегидрогеназы на глутамат.
Образование аминокислот
Глютамин синтезируется из глутамата глутаминсинтетазой, которая использует аденозинтрифосфат для образования глутамилфосфата; этот промежуточный продукт подвергается атаке аммиака как нуклеофила с образованием глутамина и неорганического фосфата. Пролин, аргинин и лизин (у некоторых организмов) также являются синтезируемыми другими аминокислотами. Эти три аминокислоты получают из глутамата с добавлением дополнительных стадий или ферментов для облегчения реакций.
Переносчик азота
Другая функция заключается в объединении с азотом , высвобождаемым в клетках, что предотвращает перегрузку азотом.
α-Кетоглутарат является одним из наиболее важных переносчиков азота в метаболических путях. Аминогруппы аминокислот присоединяются к нему (посредством трансаминирования ) и переносятся в печень, где имеет место цикл мочевины .
α-Кетоглутарат трансаминируется вместе с глутамином с образованием возбуждающего нейротрансмиттераглутамата . Затем глутамат может быть декарбоксилирован (для этого требуется витамин B 6) в ингибирующий нейромедиатор гамма-аминомасляную кислоту .
. Сообщается, что высокое содержание аммиака и / или высокий уровень азота может возникать при высоком потреблении белка , чрезмерном воздействии алюминия, синдроме Рея , циррозе и нарушении цикла мочевины .
роль в детоксикации аммиака в головном мозге.
Связь с молекулярным кислородом
Действуя как вспомогательный субстрат для α-кетоглутарат-зависимой гидроксилазы , он также играет важную функцию в реакциях окисления с участием молекулярного кислорода.
Молекулярный кислород (O 2 ) непосредственно окисляет многие соединения с образованием полезных продуктов в организме, таких как антибиотики , в реакциях, катализируемых оксигеназы . Во многих оксигеназах α-кетоглутарат помогает реакции, окисляясь основным субстратом . EGLN1 , одна из α-кетоглутарат-зависимых оксигеназ, представляет собой датчик O 2 , информирующий организм об уровне кислорода в окружающей его среде.
В сочетании с молекулярным кислород, альфа-кетоглутарат является одним из требований для гидроксилирования пролина до гидроксипролина при производстве типа 1 коллагена .
Антиоксидант
α-кетоглутарат, который выделяется несколькими типами клеток, уменьшается уровни перекиси водорода и α-кетоглутарата были истощены и преобразованы в сукцинат в средах для культивирования клеток.
Долголетие
Исследования высвободили связанный α-кетоглутарат с увеличенной продолжительностью жизни у нематодных червей и увеличение продолжительности здоровья / продолжительности жизни у мышей.
Иммунная регуляция
Исследование показало, что α-кетоглутарат способствует дифференцировке TH1 и истощению глютамина (за счет истощения его метаболита, α-кетоглутарат способствует treg (регуляторные Т-клетки) дифференцировка. Это может сыграть роль в смещении баланса в пользу трегов в условиях аминокислотной депривации, которую можно наблюдать в микроокружении опухоли.
Продукция
α-кетоглутарат может быть произведен:
- окислительным декарбоксилированием изоцитрат изоцитратдегидрогеназой
- Окислительное дезаминирование глутамата глутаматдегидрогеназой
- Из галактуроновой кислоты организмом Agrobacterium tumefaciens
Альфа-кетоглутарат может использоваться для производства:
- Креатина-альфа-кетоглутарата
Интерактивная карта путей
Щелкните гены, белки и метаболиты ниже, чтобы ссылаться на соответствующие статьи.
См. Также
- 2OG-зависимые диоксигеназы
Ссылки
Источник
| Имена | |
|---|---|
| Предпочтительное название IUPAC 2-оксопентандиовая кислота | |
| Другие названия 2-кетоглутаровая кислота, альфа-кетоглутаровая кислота, 2-оксоглутаровая кислота, оксоглутаровая кислота. | |
| Идентификаторы | |
Количество CAS |
|
3D модель ( JSmol ) |
|
| ЧЭБИ |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA Card | 100.005.756 |
IUPHAR / BPS |
|
| КЕГГ |
|
| MeSH | альфа-кетоглутаровая + кислота |
PubChem CID |
|
| UNII |
|
Панель управления CompTox ( EPA ) |
|
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
Химическая формула | С 5 Н 6 О 5 |
| Молярная масса | 146,11 г / моль |
| Температура плавления | 115 ° С (239 ° F, 388 К) |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| проверить ( что есть ?) | |
| Ссылки на инфобоксы | |
α-Кетоглутаровая кислота ( 2-оксоглутаровая кислота ) является одним из двух кетоновых производных глутаровой кислоты . Термин «кетоглутаровая кислота», если он не уточняется, почти всегда относится к альфа-варианту. β-Кетоглутаровая кислота варьируется только положением функциональной группы кетона и встречается гораздо реже.
Его анион , α-кетоглутарат, также называемый 2-оксоглутаратом , является важным биологическим соединением. Это кето кислоты получают путем дезаминирования из глутамата , и является промежуточным продуктом в цикле Кребса .
Функции
Аланин трансаминаза
Фермент аланинаминотрансфераза преобразует α-кетоглутарат и L – аланин с L -glutamate и пируват , соответственно, в качестве обратимого процесса.
Цикл Кребса
α-Кетоглутарат является ключевым промежуточным продуктом в цикле Кребса , идущим после изоцитрата и до сукцинил-КоА . Анаплеротические реакции могут восполнить цикл на этом этапе путем синтеза α-кетоглутарата путем трансаминирования глутамата или посредством действия глутаматдегидрогеназы на глутамат.
Образование аминокислот
Глутамин синтезируется из глутамата глутамин синтетазой, которая использует аденозинтрифосфат для образования глутамилфосфата; это промежуточное соединение подвергается атаке аммиака как нуклеофила, дающего глутамин и неорганический фосфат. Пролин, аргинин и лизин (у некоторых организмов) также являются синтезируемыми другими аминокислотами. Эти три аминокислоты получают из глутамата с добавлением дополнительных стадий или ферментов для облегчения реакций.
Транспортер азота
Другая функция – объединение с азотом, высвобождаемым в клетках, тем самым предотвращая перегрузку азотом.
α-Кетоглутарат – один из важнейших переносчиков азота в метаболических путях. Аминогруппы аминокислот присоединяются к нему (путем трансаминирования ) и переносятся в печень, где происходит цикл мочевины .
α-Кетоглутарат трансаминируется вместе с глутамином с образованием возбуждающего нейромедиатора глутамата . Затем глутамат может быть декарбоксилирован (для чего требуется витамин B 6 ) в ингибирующий нейромедиатор гамма-аминомасляную кислоту .
Сообщается, что высокий уровень аммиака и / или высокий уровень азота может возникать при высоком потреблении белка , чрезмерном воздействии алюминия, синдроме Рейе , циррозе и нарушении цикла мочевины .
Он играет роль в детоксикации аммиака в головном мозге.
Связь с молекулярным кислородом
Действуя как вспомогательный субстрат для α-кетоглутарат-зависимой гидроксилазы , он также играет важную роль в реакциях окисления с участием молекулярного кислорода.
Молекулярный кислород (O 2 ) непосредственно окисляет многие соединения с образованием полезных продуктов в организме, таких как антибиотики , в реакциях, катализируемых оксигеназами . Во многих оксигеназах α-кетоглутарат помогает реакции, окисляясь основным субстратом . EGLN1 , одна из α-кетоглутарат-зависимых оксигеназ, является сенсором O 2 , информирующим организм об уровне кислорода в окружающей его среде.
В сочетании с молекулярным кислородом альфа-кетоглутарат является одним из требований для гидроксилирования пролина до гидроксипролина при производстве коллагена 1 типа .
Антиоксидант
α-Кетоглутарат, который выделяется несколькими типами клеток, снижает уровень перекиси водорода , а α-кетоглутарат истощается и превращается в сукцинат в средах для культивирования клеток.
Долголетие
Исследования показали, что α-кетоглутарат связан с увеличением продолжительности жизни нематодных червей и увеличением продолжительности жизни / здоровья мышей.
Иммунная регуляция
Исследование показало, что в условиях отсутствия глутамина α-кетоглутарат способствует дифференцировке наивных CD4 + Т-клеток в TH1, одновременно подавляя их дифференцировку в противовоспалительные Treg-клетки.
Производство
α-Кетоглутарат может производиться:
- Окислительное декарбоксилирование из изоцитрата по изоцитратдегидрогеназы
- Окислительное дезаминирование из глутамата с помощью глутаматдегидрогеназы
- Из галактуроновой кислоты организмом Agrobacterium tumefaciens
Альфа-кетоглутарат можно использовать для производства:
- Креатин-альфа-кетоглутарат
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.
[[Файл:
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
[[]]
| alt = TCACycle_WP78 править ]]
Смотрите также
- 2OG-зависимые диоксигеназы
Рекомендации
Источник